ANGBEBOTE
BESTELLUNG
Angebote
ZOVIRAX Lippenherpes Creme 2 g *
- Anbieter:
- GlaxoSmithKline Consumer Healthcare
- Einheit:
- 2 g Creme
- PZN:
- 02799289
- Verfügbarkeit:
- Gewöhnlich versandfertig in 1-2 Tagen.
- Ihr Preis:¹
- 8,85 €¹
- UVP:³
- 11,64 €³
- Sie sparen:
- 2,79 € (24%)
Gewöhnlich versandfertig in 1-2 Tagen.
Rabatt -24%
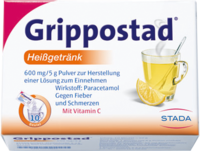
GRIPPOSTAD Heißgetränk Pulver 10 St *
- Anbieter:
- STADA Consumer Health Deutschland GmbH
- Einheit:
- 10 St Pulver
- PZN:
- 04548551
- Verfügbarkeit:
- Gewöhnlich versandfertig in 1-2 Tagen.
- Ihr Preis:¹
- 10,77 €¹
- AVP:²
- 11,97 €²
- Sie sparen:
- 1,20 € (10%)
Gewöhnlich versandfertig in 1-2 Tagen.
Rabatt -10%
ASPIRIN plus C Brausetabletten 10 St *
- Anbieter:
- Bayer Vital GmbH
- Einheit:
- 10 St Brausetabletten
- PZN:
- 01406632
- Verfügbarkeit:
- Gewöhnlich versandfertig in 1-2 Tagen.
- Ihr Preis:¹
- 7,95 €¹
- AVP:²
- 8,48 €²
- Sie sparen:
- 0,53 € (6,2%)
Gewöhnlich versandfertig in 1-2 Tagen.
Rabatt -6,2%
VOLTAREN Schmerzgel 1,16% Gel Komf.-Applikator 100 g *
- Anbieter:
- GlaxoSmithKline Consumer Healthcare
- Einheit:
- 100 g Gel
- PZN:
- 12732027
- Verfügbarkeit:
- Gewöhnlich versandfertig in 1-2 Tagen.
- Ihr Preis:¹
- 13,56 €¹
- AVP:²
- 15,07 €²
- Sie sparen:
- 1,51 € (10%)
- Grundpreis:
- ( 135,60 € pro 1 kg )
Gewöhnlich versandfertig in 1-2 Tagen.
Rabatt -10%
NASENSPRAY-ratiopharm Erwachsene kons.frei 15 ml *
- Anbieter:
- ratiopharm GmbH
- Einheit:
- 15 ml Nasenspray
- PZN:
- 00999848
- Verfügbarkeit:
- Nicht lieferbar.
- Ihr Preis:¹
- 4,95 €¹
- UVP:³
- 6,97 €³
- Sie sparen:
- 2,02 € (29%)
- Grundpreis:
- ( 330,00 € pro 1 l )
Nicht lieferbar.
Rabatt -29%
WICK MediNait Erkält.Sirup m.Honig-u.Kamillenaroma 120 ml *
- Anbieter:
- WICK Pharma - Zweigniederlassung der Procter & Gamble GmbH
- Einheit:
- 120 ml Sirup
- PZN:
- 06156393
- Verfügbarkeit:
- Nicht lieferbar.
- Ihr Preis:¹
- 15,35 €¹
- Grundpreis:
- ( 127,92 € pro 1 l )
Nicht lieferbar.
Topseller
LIVSANE B12 Vital Power Trinkampullen 10X10 ml
- Anbieter:
- PXG Pharma GmbH
- Einheit:
- 10X10 ml Trinkampullen
- PZN:
- 15415847
- Verfügbarkeit:
- Gewöhnlich versandfertig in 1-2 Tagen.
- Ihr Preis:¹
- 10,95 €¹
- UVP:³
- 16,99 €³
- Sie sparen:
- 6,04 € (35,6%)
- Grundpreis:
- ( 109,50 € pro 1 l )
Gewöhnlich versandfertig in 1-2 Tagen.
Rabatt -35,6%
ORTHOMOL Immun Trinkfläschchen/Tabl.Kombipack. 30 St
- Anbieter:
- Orthomol pharmazeutische Vertriebs GmbH
- Einheit:
- 30 St Trinkampullen
- PZN:
- 01319991
- Verfügbarkeit:
- Gewöhnlich versandfertig in 24 Stunden.
- Ihr Preis:¹
- 54,95 €¹
- UVP:³
- 69,99 €³
- Sie sparen:
- 15,04 € (21,5%)
Gewöhnlich versandfertig in 24 Stunden.
Rabatt -21,5%
GRIPPOSTAD C Hartkapseln 24 St *
- Anbieter:
- STADA Consumer Health Deutschland GmbH
- Einheit:
- 24 St
- PZN:
- 00571748
- Verfügbarkeit:
- Gewöhnlich versandfertig in 1-2 Tagen.
- Ihr Preis:¹
- 12,95 €¹
- AVP:²
- 16,37 €²
- Sie sparen:
- 3,42 € (20,9%)
Gewöhnlich versandfertig in 1-2 Tagen.
Rabatt -20,9%
IBUDOLOR akut 400 mg Filmtabletten 20 St *
- Anbieter:
- STADA Consumer Health Deutschland GmbH
- Einheit:
- 20 St Filmtabletten
- PZN:
- 09091257
- Verfügbarkeit:
- Gewöhnlich versandfertig in 1-2 Tagen.
- Ihr Preis:¹
- 4,95 €¹
- AVP:²
- 6,38 €²
- Sie sparen:
- 1,43 € (22,4%)
Gewöhnlich versandfertig in 1-2 Tagen.
Rabatt -22,4%
HYLO-COMOD Augentropfen 10 ml
- Anbieter:
- URSAPHARM Arzneimittel GmbH
- Einheit:
- 10 ml Augentropfen
- PZN:
- 00495970
- Verfügbarkeit:
- Gewöhnlich versandfertig in 1-2 Tagen.
- Ihr Preis:¹
- 10,95 €¹
- UVP:³
- 15,95 €³
- Sie sparen:
- 5,00 € (31,3%)
- Grundpreis:
- ( 1.095,00 € pro 1 l )
Gewöhnlich versandfertig in 1-2 Tagen.
Rabatt -31,3%
VOLTAREN Schmerzgel forte 23,2 mg/g 180 g *
- Anbieter:
- GlaxoSmithKline Consumer Healthcare
- Einheit:
- 180 g Gel
- PZN:
- 11240397
- Verfügbarkeit:
- Gewöhnlich versandfertig in 1-2 Tagen.
- Ihr Preis:¹
- 22,95 €¹
- AVP:²
- 33,64 €²
- Sie sparen:
- 10,69 € (31,8%)
- Grundpreis:
- ( 127,50 € pro 1 kg )
Gewöhnlich versandfertig in 1-2 Tagen.
Rabatt -31,8%
NASENSPRAY-ratiopharm Erwachsene kons.frei 15 ml *
- Anbieter:
- ratiopharm GmbH
- Einheit:
- 15 ml Nasenspray
- PZN:
- 00999848
- Verfügbarkeit:
- Nicht lieferbar.
- Ihr Preis:¹
- 4,95 €¹
- UVP:³
- 6,97 €³
- Sie sparen:
- 2,02 € (29%)
- Grundpreis:
- ( 330,00 € pro 1 l )
Nicht lieferbar.
Rabatt -29%